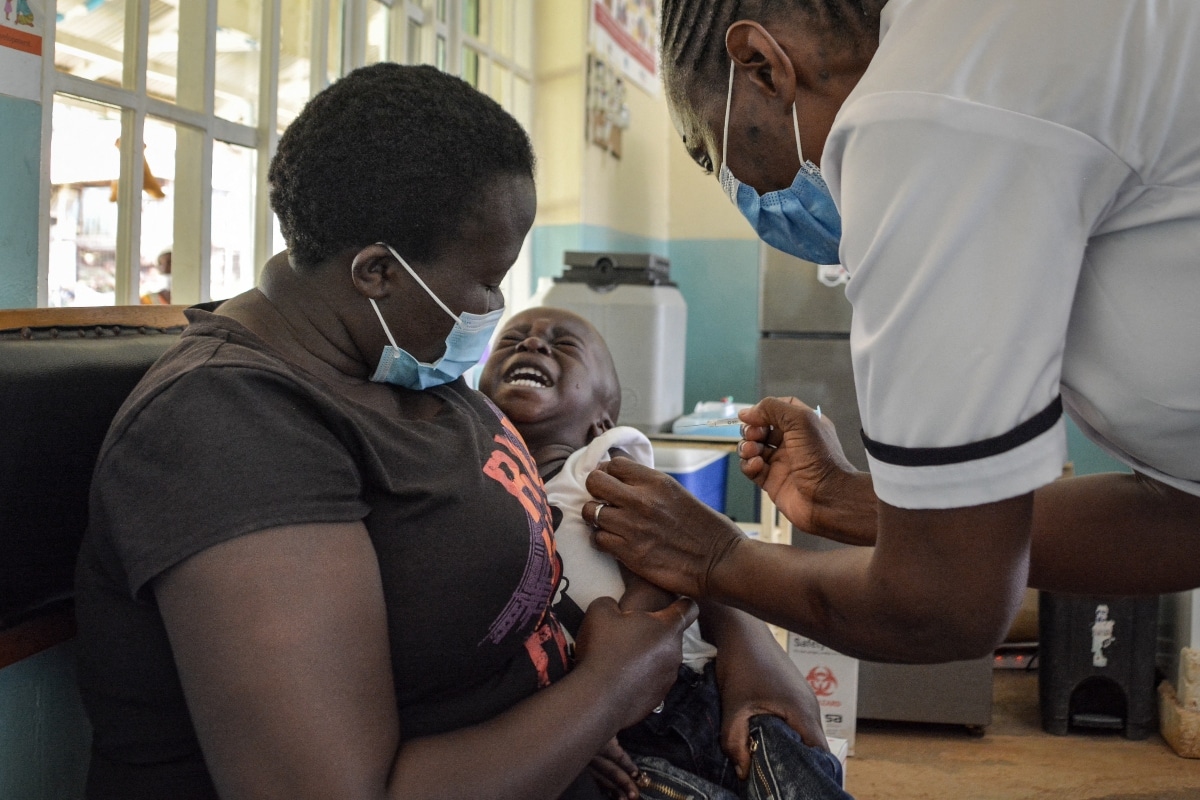
Los avances en materia de vacunación se anotaron esta semana dos victorias: la primera, ante la Organización Mundial de la Salud (OMS) al conseguir la aprobación de un biológico en contra de la malaria; y la segunda con la solicitud formal ante la FDA estadounidense para autorizar el uso de emergencia de la vacuna contra el Covid-19 en niños de 5 a 11 años. En ambos casos, los menores son los beneficiados.
TE PUEDE INTERESAR: Más de 30 heridos en un terremoto de 6,1 grados en la región de Tokio
Para la malaria, la sustancias llamada “RTS,S” -aprobada de forma generalizada-, reduce 30% los efectos en su forma más grave, según Kate O’Brien, directora del departamento de Vacunación de la OMS.
Esta enfermedad, considerada como una de las más mortíferas del mundo y que se manifiesta a través de fiebre, dolores de cabeza y musculares, cobra casi medio millón de vidas al año, de las que 260 mil corresponden a niños menores de cinco años.
Detrás de este desarrollo se encuentra la alemana BioNTech, que utilizó tecnología de ARN mensajero, como en el caso de su versión contra el Covid-19, para lo cual se alió con la farmacéutica estadounidense Pfizer.
TE PUEDE INTERESAR: Pfizer solicita autorización de vacuna Covid-19 para niños de 5 a 11 años
Al mismo tiempo, ayer se presentó una petición formal ante la Administración de Medicamentos y Alimentos (FDA) de EU por parte de los laboratorios antes mencionados para la autorización de emergencia de la dosis reducida contra Covid-19 en niños de 5 a 11 años. Esto después de reportar ante la institución los resultados finales de sus ensayos, en los que observaron que la vacuna fue bien tolerada y provoca una respuesta inmune comparable con la que registraron personas de 16 a 25 años.
La FDA programó una reunión el próximo 26 de octubre con su comité asesor, que opinará antes de que se conceda oficialmente la autorización para comenzar las campañas correspondientes.
LEG